En química, se conoce como hibridación a la interacción de orbitales atómicos dentro de un átomo para formar nuevos orbitales híbridos. Los orbitales atómicos híbridos son los que se superponen en la formación de los enlaces, dentro de la teoría del enlace de valencia, y justifican la geometría molecular. Por lo tanto podemos decir que la hibridación es una herramienta teórica que ayuda a entender la estructura y el comportamiento de las moléculas en términos de sus enlaces químicos
El químico Linus Pauling desarrolló por primera vez la teoría de la hibridación con el fin de explicar la estructura de las moléculas como el metano (CH4) en 1931.[1] Este concepto fue desarrollado para este tipo de sistemas químicos sencillos, pero el enfoque fue más tarde aplicado más ampliamente, y hoy se considera una heurística eficaz para la racionalización de las estructuras de compuestos orgánicos.
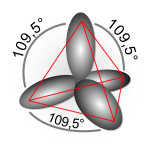
Hibridación sp3
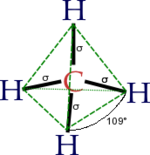
El átomo de carbono tiene seis electrones: dos se ubican en el orbital (1s²), dos en el (2s²) y los restantes dos en el orbital 2p (2p²). Debido a su orientación en el plano tridimensional el subnivel 2p tiene capacidad para ubicar 6 electrones: 2 en el orbital px, dos en el orbital py y dos electrones en el orbital pz. Los dos últimos electrones del carbono se ubicarían uno en el 2px, el otro en el 2py y el orbital 2pz permanece vacío (2px¹ 2py¹). El esquema de lo anterior es (cada flecha un electrón):
Para satisfacer su energético inestable, un átomo de valencia como el del carbono, con orbitales parcialmente llenos (2px y 2py necesitarían tener dos electrones) tiende a formar enlaces con otros átomos que tengan electrones disponibles. Para ello, no basta simplemente colocar un electrón en cada orbital necesitado. En la naturaleza, este tipo de átomos redistribuyen sus electrones formando orbitales híbridos. En el caso del carbono, uno de los electrones del orbital 2s es extraído y se ubica en el orbital 2pz. Así, los cuatro últimos orbitales tienen un electrón cada uno:
El estímulo para excitar al electrón del 2s al 2pz es aportado por el primer electrón en formar enlace con un átomo con este tipo de valencia. Por ejemplo, el hidrógeno en el caso del metano. Esto a su vez incrementa la necesidad de llenado de los restantes orbitales. Estos nuevos orbitales híbridos dejan de ser llamados 2s y 2p y son ahora llamados sp3 (un poco de ambos orbitales):
De los cuatro orbitales así formados, uno (un 25%) es proveniente del orbital s (el 2s) del carbono y tres (un 75%) provenientes de los orbitales p (2p). Sin embargo todos se sobreponen al aportar la hibridación producto del enlace. Tridimensionalmente, la distancia entre un hidrógeno y el otro en el metano son equivalentes e iguales a un ángulo de 109,5°.
Hibridación sp2

Se define como la combinación de un orbital s y dos orbitales p, para formar 3 orbitales híbridos, que se disponen en un plano formando ángulos de 120° grados.
Los átomos que forman hibridaciones sp2 pueden formar compuestos con enlaces dobles. Forman un ángulo de 120° y su molécula es de forma plana. A los enlaces simples se les conoce como enlaces sigma (σ) y los enlaces dobles están compuestos por un enlace sigma y un enlace pi (). Las reglas de ubicación de los electrones en estos casos, como el alqueno etileno obligan a una hibridación distinta llamada sp2, en la cual un electrón del 2s se mezcla solo con dos de los orbitales 2p: surge a partir o al unirse el orbital s con dos orbitales p; por consiguiente, se producen tres nuevos orbitales sp2, cada orbital nuevo produce enlaces covalentes
Tridimensionalmente, la distancia entre un hidrógeno y otro en algún carbono del etileno son equivalentes e iguales a un ángulo de 120°.
Hibridación sp

Se define como la combinación de un orbital s y un orbital p, para formar 2 orbitales híbridos, con orientación lineal.
Este es el tipo de enlace híbrido, con un ángulo de 180° y que se encuentra existente en compuestos con triples enlaces como los alquinos (por ejemplo el acetileno):
Se caracteriza por la presencia de 2 enlaces pi (π).
Forma y ángulos
Las formas de las moléculas enlazadas por hibridaciones de sus orbitales es forzada por los ángulos entre sus átomos:

| molécula de tipo | hibridación spx | hibridación sdx | hibridación spxdy |
|---|---|---|---|
| elemento representativo/ metales de transición |
solo metales de transición | ||
| AX2 |
|
||
| AX3 |
|
|
|
| AX4 |
|
|
|
| AX6 |
|
| |
| ángulos interorbitales | |||
El enlace hipervalente también ha sido descrito como orbitales híbridos sp3d y sp3d2, compuestos de orbitales s, p, y d a niveles de energía más altos. Sin embargo, avances en el estudio de cálculos ab initio han revelado que la contribución de los orbitales d al enlace hipervalente es demasiado pequeña para describir las propiedades del enlace, y esta descripción por orbitales híbridos es vista como muy poco importante.[2][3] Estas moléculas usan resonancia.
| AX5 | bipiramidal trigonal |
|---|---|

| |
| AX6 | octaédrica |
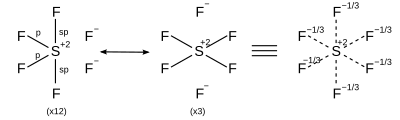
| |
| AX7 | bipiramidal pentagonal |
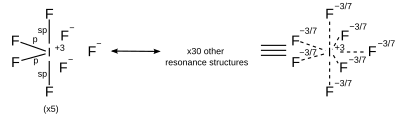
|
Véase también
Referencias
- ↑ Pauling, L. (1931), «The nature of the chemical bond. Application of results obtained from the quantum mechanics and from a theory of paramagnetic susceptibility to the structure of molecules», Journal of the American Chemical Society 53 (4): 1367-1400, doi:10.1021/ja01355a027.
- ↑ Magnusson, E. (1990). "Hypercoordinate molecules of second-row elements: d functions or d orbitals?". J. Am. Chem. Soc. 112 (22): 7940–7951. doi 10.1021/ja00178a014
- ↑ David L. Cooper; Terry P. Cunningham; Joseph Gerratt; Peter B. Karadakov; Mario Raimondi (1994). "Chemical Bonding to Hypercoordinate Second-Row Atoms: d Orbital Participation versus Democracy". Journal of the American Chemical Society. 116 (10): 4414–4426. doi 10.1021/ja00089a033
















