La hidroformilación, también conocida como síntesis oxo o proceso oxo, es un proceso importante para la producción industrial de aldehídos a partir de alquenos.[1] Esta reacción química implica la adición de un grupo formilo (-CHO) y un átomo de hidrógeno sobre un enlace doble carbono-carbono. Este proceso ha experimentado un crecimiento continuo desde su invención en la década de 1930: la capacidad de producción llegó a 6,6×106 toneladas en 1995. Es importante porque los aldehídos resultantes se convierten fácilmente en muchos productos secundarios. Por ejemplo, los aldehídos resultantes son hidrogenados a alcoholes que se convierten en detergentes. La hidroformilación también se utiliza en productos químicos especiales, importantes a la síntesis orgánica de fragancias y productos naturales. El desarrollo de la hidroformilación, que se originó por Otto Roelen en la industria alemana del carbón hacia 1930, es considerado uno de los logros principales de la química industrial del siglo XX.
El proceso normalmente se lleva a cabo el tratamiento de un alqueno con monóxido de carbono e hidrógeno a altas presiones (entre 10 y 100 atmósferas) y a temperaturas entre 40 y 200 °C. Es necesario el empleo de catalizadores con base en metales de transición.
Catalizadores
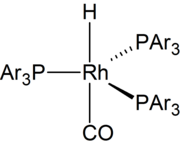
El catalizador original era HCo(CO)4, descubierto por Otto Roelen[2][3] Trabajos posteriores demostraron que el ligando tributilfosfina (PBu3) mejoraba la selectividad del proceso catalizado por cobalto. Desde la década de 1970, la mayoría de hidroformilaciones se realizan con catalizadores basados en rodio.[4][5] La investigación posterior condujo al desarrollo de catalizadores solubles en agua que facilitaban la separación de los productos del catalizador.[6]
Mecanismo
El mecanismo general se asemeja a la hidrogenación homogénea con etapas adicionales. La reacción se inicia con la generación de complejos de hidruros de carbonilo metálico coordinativamente insaturados tales como HCO(CO)3 y SAR(CO)(PPh3)2. Estas especies se unen a alquenos, y el complejo resultante se somete a una reacción de inserción migratoria para formar un complejo de alquilo.
Selectividad
Una consideración clave de la hidroformilación es la selectividad "normal" frente a "iso". Por ejemplo, la hidroformilación de propileno puede formar dos productos isómeros, butiraldehído o isobutiraldehído:
- H2 + CO + CH3CH=CH2 → CH3CH2CH2CHO ("normal")
- vs.
- H2 + CO + CH3CH=CH2 → (CH3)2CHCHO ("iso")
Estos isómeros son el resultado de las diferentes formas de inserción del alqueno en el enlace M-H. Por supuesto, ambos productos no son igualmente válidos. Se han dedicado muchas investigaciones a la búsqueda de catalizadores que favorezcan el isómero normal.
Efectos estéricos
Cuando el hidrógeno se transfiere al átomo de carbono que posee más átomos de hidrógeno (adición de Markovnikov) el grupo alquilo resultante tiene un gran impedimento estérico próximo a los ligandos sobre el cobalto. Si los ligandos unidos al cobalto son voluminosos (como el grupo tributilfosfina), este efecto estérico es mayor. De ahí que los complejos de carbonilo/fosfina mezclados ofrezcan una mayor selectividad hacia los productos de cadena lineal.

Efectos electrónicos
Además, cuanto más rico en electrones sea el complejo hidruro, menos protones como el hidruro posee, por tanto, como resultado de los efectos electrónicos que favorecen la adición de Markovnikov a un alqueno, son menos capaces de dirigir el hidruro al átomo de carbono que ya tiene más átomos de hidrógeno. Así como resultado cuando el centro metálico se vuelve más rico en electrones, el catalizador se vuelve más selectivo para los compuestos de cadena lineal.
Formación de acetilo
Después de la formación de alquilo, una segunda inserción migratoria convierte el grupo alquilo en un ligando acetilo (esto ocurre cuando el carbono alquílico forma un enlace con el carbono de un ligando carbonilo). El sitio vacante en el metal es llenado por dos átomos de hidrógeno (a partir de la inserción oxidativa de una molécula de hidrógeno). Una de estos hidruros luego toma parte en una eliminación reductora para formar la molécula de aldehído y el complejo [HCO(CO)3].

Es importante que la tasa de inserción migratoria del carbonilo en el enlace carbono-metal del grupo alquilo sea rápida; en sistemas donde la inserción migratoria no tiene lugar (como el hidruro de tristrifenilfosfitoníquel), la reacción del hidruro con el alqueno es reversible. Esto da como resultado la isomerización del alqueno, de esta manera el oct-2-eno se podría convertir en una mezcla de oct-1-eno y oct-2-eno mediante una eliminación de hidruro beta del grupo alquilo. En el sistema, por debajo de la tasa de inserción del carbono carbonilo en el enlace C-M es probable que sea mayor que la tasa de eliminación de beta-hidruro. Si ocurriera lo contrario entonces algo de n-C8H17CHO se habría formado.[7]
Hidroformilación de 2-octeno: el catalizador de rodio se coordina con el acac y el monóxido de carbono y se encapsula en un proceso de autoensamblaje molecular por la tetrafenilporfirina de zinc o Zn-TPP y el análogo de piridina con trifenilfosfina. En este proceso, muy parecido a la forma en que las enzimas realizan la encapsulación del sitio catalítico, se explica la regioselectividad observada:

Hidroformilación asimétrica
La hidroformilación de alquenos internos crea nuevos estereocentros. Usando ligandos fosfina quirales, la hidroformilación se pueden adaptar en favor de un enantiómero.[8]
Otros sustratos
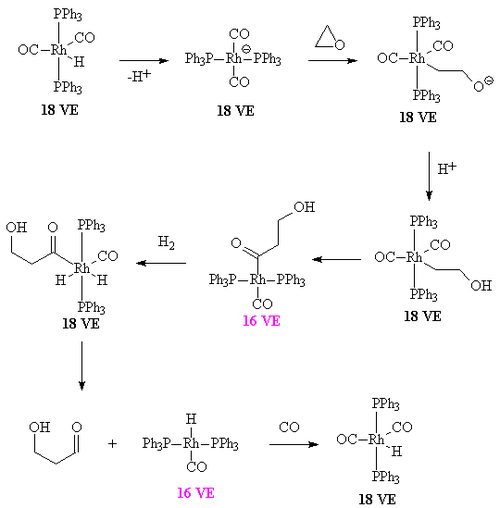
Los complejos carbonilo de cobalto y de rodio catalizan la hidroformilación del formaldehído y el óxido de etileno para dar 2-hidroxiacetaldehído y 3-hidroxipropanaldehído, que luego pueden ser hidrogenados para dar etilenglicol y 1,3-propanodiol, respectivamente. Las reacciones son más eficaces cuando el disolvente es básico (por ejemplo, piridina ).[9][10]
En el caso del octacarbonilo de dicobalto o Co2(CO)8 como catalizador, se puede obtener 2-pentanona a partir de etileno y CO, en ausencia de hidrógeno. Un intermedio propuesto es la especie etilen-propionilo [CH3C(O)Co(CO)3(etileno)], que se somete a un inserción migratoria para formar [CH3COCH2CH2Co(CO)3]. El hidrógeno que se requiere se deriva de la reacción de desplazamiento de agua. Para más detalles véase[11]

Si la reacción de desplazamiento del agua no es operativa, la reacción proporciona un polímero que contiene monóxido de carbono y alternando unidades de etileno. Tales polímeros son más preparados convencionalmente con catalizadores de paladio.[12]
Enlaces externos
- 3.1.1. Fundamentos químicos de la hidroformilación. En: Curso de Química Orgánica I. Facultad de Química. Química Orgánica. UNAM.
Referencias
- ↑ Ojima, I.; Tsai, C.-Y.; Tzamarioudaki, M.; Bonafoux, D. Org. React. 2000, 56, 1. (doi: 10.1002/0471264180.or056.01)
- ↑ Boy Cornils, Wolfgang A. Herrmann, Manfred Rasch (1994). «Otto Roelen, Pioneer in Industrial Homogeneous Catalysis». Angewandte Chemie International Edition in English 33 (21): 2144-2163. doi:10.1002/anie.199421441.
- ↑ [1]
- ↑ Imyanitov N.S., Rudkovskij D.M. (1963). «Hydrogenation and hydroformylation in the presence of Co, Rh, and Ir carbonyls». Neftekhimiya (Rus) 3 (2): 198-200.
- ↑ Evans D., Osborn J. A., Wilkinson G. (1968). «Hydroformylation of Alkenes by Use of Rhodium Complex Catalyst». Journal of the Chemical Society 33 (21): 3133-3142. doi:10.1039/J19680003133.
- ↑ Cornils, B.; Herrmann, W. A. (eds.) “Aqueous-Phase Organometallic Catalysis” VCH, Weinheim: 1998
- ↑ High-Precision Catalysts: Regioselective Hydroformylation of Internal Alkenes by Encapsulated Rhodium Complexes Kuil, M.; Soltner, T.; van Leeuwen, P. W. N. M.; Reek, J. N. H. Journal of the American Chemical Society; 2006; 128(35) pp 11344 - 11345; doi 10.1021/ja063294i
- ↑ Watkins, A. L.; Hashiguchi, B. G.; Landis, C. R., Highly Enantioselective Hydroformylation of Aryl Alkenes with Diazaphospholane Ligands. Organic Letters 2008, 10 (20), 4553-4556.
- ↑ Chan A.S.C., Shieh H-S. (1994). «A mechanistic study of the homogeneous catalytic hydroformylation of formaldehyde: synthesis and characterization of model intermediates». Inorganica Chimica Acta 218 (1-2): 89-95. doi:10.1016/0020-1693(94)03800-7.
- ↑ Spencer A. (1980). «Hydroformylation of formaldehyde catalysed by rhodium complexes». Journal of Organometallic Chemistry 194 (1-2): 113-123. doi:10.1016/S0022-328X(00)90343-7.
- ↑ Murata K., Matsuda A., (1981). «Application of Homogeneous Water-Gas Shift Reaction III Further Study of the Hydrocarbonylation - A highly Selective Formation of Diethyl Keton from Ethene, CO and H2O». Bulletin of the Chemical Society Japan 54 (7): 2089-2092. doi:10.1246/bcsj.54.2089.
- ↑ J. Liu, B.T. Heaton, J.A. Iggo and R. Whyman, Angew. Chem. Int. Ed., 2004, 43, 90-94
Bibliografía
- 9.3 Hidroformulación de alquenos. En: Química organometálica de los metales de transición. Robert H. Crabtree. Editorial de la Universitat Jaume I, 1997. ISBN 8480211342. Pág. 292
- http://books.google.es/books?id=UxA3kcGM-i0C&pg=PA123 6.1.2. Sistema industrial de hidroformilación. En: Química orgánica industrial. Klaus Weissermel, Hans-Jürgen Arpe. Editorial Reverté, 1981. ISBN 8429179895. Pág. 123
- “Applied Homogeneous Catalysis with Organometallic Compounds: A Comprehensive Handbook in Two Volumes (Paperback) by Boy Cornils (Editor), W. A. Herrmann (Editor). ISBN 3-527-29594-1
- “Rhodium Catalyzed Hydroformylation” P. W. N. M. van Leeuwen, C. Claver Eds.; Springer; (2002). ISBN 1-4020-0421-4 (en inglés)
- “Homogeneous Catalysis: Understanding the Art” by Piet W. N. M. van Leeuwen Springer; ISBN 2005. ISBN 1-4020-3176-9 (en inglés)
- Imyanitov N.S./ Hydroformylation of Olefins with Rhodium Complexes // Rhodium Express. 1995. No 10 - 11 (May). P. 3 - 62 (Eng). ISSN 0869-7876 Archivado el 23 de junio de 2022 en Wayback Machine. (en inglés)








