| Propileno (pp) | ||
|---|---|---|
 | ||
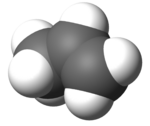 Modelo molecular tridimensional | ||
| Nombre IUPAC | ||
| Propeno | ||
| General | ||
| Otros nombres |
Propileno Metiletileno Metileteno | |
| Fórmula semidesarrollada | H2C=CH–CH3 | |
| Fórmula molecular | C3H6 | |
| Identificadores | ||
| Número CAS | 115-07-1[1] | |
| Número RTECS | UC6740000 | |
| ChEBI | 16052 | |
| ChEMBL | CHEMBL117213 | |
| ChemSpider | 7954 | |
| PubChem | 8252 | |
| UNII | AUG1H506LY | |
| KEGG | C11505 | |
| Propiedades físicas | ||
| Apariencia | Gas incoloro | |
| Densidad | 1,81 kg/m³; 1,83 g/cm³ | |
| Masa molar | 42,08 g/mol | |
| Punto de fusión | 88,3 K (−185 °C) | |
| Punto de ebullición | 225 K (−48 °C) | |
| Punto de descomposición | 342 K (69 °C) | |
| Presión crítica | 24.07 atm | |
| Presión de vapor | 1020 kPa (a 20 °C) | |
| Peligrosidad | ||
| SGA |
 | |
| Punto de inflamabilidad | 165 K (−108 °C) | |
| NFPA 704 |
4
1
1
| |
| Temperatura de autoignición | 733 K (460 °C) | |
| Frases R | R12 | |
| Frases S | S9 S16 S33 | |
| Límites de explosividad | 2,0 - 11,1% de propeno en el aire. (a 20 °C) | |
| Riesgos | ||
| Riesgos principales | Inflamable | |
| Más información | Concentración máxima permitida en los lugares de trabajo: 500 ppm (VLA-ED, ACGIH-2008). | |
| Compuestos relacionados | ||
| Alquenos | Etileno, Isómeros de Butileno | |
| Otros compuestos relacionados | Propano, 2-Propanol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El propileno o propeno (H2C=CH–CH3) es un hidrocarburo perteneciente a los alquenos, incoloro y con un débil olor similar al del petróleo, prácticamente inodoro.[2] Es un homólogo del etileno. Como todos los alquenos presenta el doble enlace como grupo funcional. Es el segundo compuesto más utilizado en la industria química en todo el mundo.[3]
Síntesis
El propeno es uno de los productos de la termólisis del petróleo. Se separa de los demás productos como el etileno por destilación a baja temperatura.
Aplicaciones
El propeno es el producto de partida en la síntesis del polipropileno.
La adición de agua en condiciones polares da iso-propanol que puede ser oxidado a la acetona. En condiciones radicalarias se obtiene n-propanol.
El ácido acrílico se produce actualmente utilizando el proceso de oxidación selectiva del propeno en dos etapas. El propeno es también un compuesto intermedio en la oxidación selectiva en una etapa de propano a ácido acrílico. Este último proceso se investiga intensivamente porque el propano es significativamente más barato en comparación con el propeno.[4][5][6][7]
Producción
Steam cracking
La tecnología dominante para producir propileno es el craqueo al vapor. La misma tecnología se utiliza para producir etileno a partir de etano. El craqueo del propano produce una mezcla de etileno, propileno, metano, hidrógeno, etc. El rendimiento de propileno es de aproximadamente el 15%. La otra materia prima principal es la nafta, especialmente en Oriente Medio y Asia.[8]. El propileno puede separarse por destilación fraccionada de mezclas de hidrocarburos obtenidas del craqueo y otros procesos de refinado; el propeno de grado de refinería es de aproximadamente 50 a 70%.[9] En Estados Unidos, el gas de esquisto es una fuente importante de propano.
Tecnología de conversión de olefinas
En la tecnología Phillips Triolefin o Tecnología de conversión de olefinas el propileno se interconvierte con etileno y 2-butenos. Se utilizan catalizadores de renio y molibdeno:[10]
La tecnología se basa en una reacción de metátesis de olefinas descubierta en Phillips Petroleum Company.[11][12] Se consiguen rendimientos de propileno de alrededor del 90 % en peso.
Está relacionado con el proceso Methanol-to-Olefins/Methanol-to-Propene. Convierte gas de síntesis (syngas) en metanol y, a continuación, convierte el metanol en etileno y/o propeno. El proceso produce agua como subproducto. El gas de síntesis se produce a partir de la reformación del gas natural o mediante la reformación inducida por vapor de productos derivados del petróleo, como la nafta, o mediante la gasificación del carbón.
Craqueo catalítico de fluidos
El craqueo catalítico en lecho fluido (FCC) de alta severidad utiliza la tecnología tradicional de FCC en condiciones severas (mayor relación catalizador/aceite, mayores tasas de inyección de vapor, temperaturas más elevadas, etc.) para maximizar la cantidad de propeno y otros productos ligeros. Una unidad de FCC de alta severidad suele alimentarse con gasóleos (parafinas) y residuos, y produce alrededor de un 20-25 m% de propeno en la materia prima junto con mayores volúmenes de gasolina de motor y subproductos destilados. Estos procesos de alta temperatura son caros y tienen una elevada huella de carbono. Por estas razones, las rutas alternativas al propileno siguen atrayendo la atención.[13]
Otros métodos comercializados
En el último siglo se han desarrollado tecnologías de producción de propileno con fines específicos. De ellas, las tecnologías de deshidrogenación del propano, como los procesos CATOFIN y OLEFLEX, se han hecho comunes, aunque siguen constituyendo una minoría del mercado, y la mayor parte de la olefina procede de las tecnologías de craqueo antes mencionadas. Los catalizadores de platino, cromo y vanadio son habituales en los procesos de deshidrogenación del propano.
Mercado e investigación
La producción de propeno se ha mantenido estática en torno a los 35 millones de toneladas (solo Europa y Norteamérica) de 2000 a 2008, pero ha ido aumentando en Asia oriental, sobre todo en Singapur y China.[14] La producción mundial total de propeno es actualmente aproximadamente la mitad de la de etileno.
Se ha explorado el uso de enzimas de ingeniería, pero no se ha comercializado.[15]
Se está investigando el uso de catalizadores portadores de oxígeno para la deshidrogenación oxidativa del propano. Esto presenta varias ventajas, ya que este mecanismo de reacción puede producirse a temperaturas más bajas que la deshidrogenación convencional, y puede no estar limitado por el equilibrio. Esto podría permitir alcanzar conversiones mucho mayores y eliminar la necesidad de una corriente de reciclado con una costosa etapa de separación de propano/propileno.
Reacciones


1) Reacción de Simmons-Smith
El diyodometano en una aleación de zinc y cobre forma el carbenoide yoduro de yodometil zinc (CH2IZnI).[16] Mediante un mecanismo de cicloadición se adiciona un grupo metilo al propeno produciéndose el metilciclopropano (como mezcla racémica R y S). La reacción ocurre con buenos rendimientos.[16]
2) Hidrogenación
El propeno en presencias hidrógeno y de un catalizador (comúnmente Pd/C o PtO2 llamado catalizador de Adams) se reduce completamente a propano.[16] La adición electrofílica ocurre con estereoquímica syn.[16]
3) Hidrohalogenación
La hidrohalogenación ocurre al hacer burbujear un halogenuro de hidrógeno en un recipiente conteniendo propeno en éter.[16] Como producto principal de la reacción se obtendrá el 2-halógenopropano (P.Ej: utilizando HBr se obtiene el 2-bromopropano).
4) Hidrohalogenación en presencia de peróxidos
Cuando la hidrohalogenación del propeno ocurre el presencia de peróxidos la regioselectividad de la reacción se invierte dando como principal producto el 1-halógenopropano (P.Ej: utilizadando HCl se obtiene el 1-cloropropano).[16]
5) Halogenación
Al hace reaccionar el propeno con un halógeno en tetraclorometano como solvente se produce el 1,2-dihalógenopropano (P.Ej: utilizando I2 se obtiene el 1,2-diyodopropano).[16]
6) Formación de halohidrinas
Cuando la halogenación se produce en presencia de agua se produce el 1-halógeno-2-propanol (P.Ej: utilizando Br2 como halógeno se produce el 1-bromo-2-propanol).[16]
7) Adición de ácido sulfúrico
El ácido sulfúrico concentrado se adiciona al propeno por un mecanismo de adición electrofílica produciendo el sulfato ácido de isopropilo.
8) Obtención de alcoholes por oximercuración
Al tratarse con acetato de mercurio (II) en tetrahidrofurano (THF) y agua y posteriormente con borohidruro de sodio (NaBH4) se produce el 2-propanol con alto rendimiento.[16]
9) Hidroboración
Mediante el tratamiento con diborano y posterior hidrólisis oxidativa con peróxido de hidrógeno (H2O2) el medio alcalino se obtiene el alcohol Antimarkovnikov 1-propanol.[16]
10) Dihidroxilación syn
La oxidación con tetróxido de osmio (OsO4) seguido del tratamiento con bisulfito de sodio y agua produce propilenglicol (como mezcla racémica R y S).[16] También se producirá la reacción de dihidroxilación syn utilizando KMnO4 diluido en medio acuoso básico a baja temperatura.[16]
11) Obtención de epóxidos
La peroxidación del propeno con un peroxiácido (RCO3H) a temperatura ambiente produce el óxido de propileno (como mezcla racémica R y S) mediante la reacción de Prileschajew.[17][18]
Industrialmente se produce por oxidación con oxígeno en presencia de un catalizador de óxido de plata (Ag2O) a altas temperaturas (300 °C).[17]
12) Clivaje oxidativo
La oxidación violenta del propeno con KMnO4 caliente produce por clivaje oxidativo ácido acético y dióxido de carbono.[16] También se obtendrían los mismos productos por ozonólisis con ozono (O3) a bajas temperaturas (-78 °C) y posterior clivaje oxidativo con peróxido de hidrógeno (H2O2) en medio alcalino.[16]
13) Polimerización
La polimerización del propileno a polipropileno se puede llevar a cabo de forma radicalaria aunque en la polimerización catalítica se obtienen productos con mejores calidades que además son mejor controlables. Los catalizadores empleados eran originalmente del tipo Ziegler-Natta. En la actualidad se están sustituyendo por otros sistemas basados en zirconocenos.
14) Adición de diclorocarbeno
Al tratar el propeno con cloroformo y con una base fuerte como KOH se obtiene 1,1-dicloro-2-metilciclopropano (como mezcla racémica R y S).[16]
15) Ozonólisis con clivaje reductivo
Por Ozonólisis con posterior clivaje oxidativo se obtiene como productos formaldehído y acetaldehído.[16]
16) Hidroformilación
La hidroformilación del propeno con monóxido de carbono, agua y un catalizador de Co a altas presiones y temperaturas produce butanal como principal producto.[19]
Usos
El propeno es el segundo producto de partida más importante en la industria petroquímica después del etileno. Es la materia prima de una gran variedad de productos. Los fabricantes de polipropileno consumen casi dos tercios de la producción mundial.[20] Los usos finales del polipropileno incluyen películas, fibras, envases, embalajes y tapas y cierres. El propeno también se utiliza para la producción de importantes productos químicos como óxido de propileno, acrilonitrilo, cumeno, butiraldehído y ácido acrílico. En el año 2013 se procesaron unos 85 millones de toneladas de propeno en todo el mundo.[20]
El propeno y el benceno se convierten en acetona y fenol mediante el proceso del cumeno.
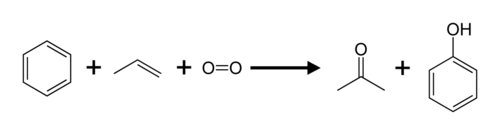
El propeno también se utiliza para producir isopropanol (propan-2-ol), acrilonitrilo, óxido de propileno y epiclorhidrina.[21] La producción industrial de ácido acrílico implica la oxidación parcial catalítica del propeno.[22] El propileno es un intermedio en la oxidación a ácido acrílico.
En la industria y los talleres, el propileno se utiliza como combustible alternativo al acetileno en soldadura por combustión (autógena), soldadura fuerte y calentamiento de metales para doblarlos. Se ha convertido en un estándar en los productos BernzOmatic y otros en sustitutos del MAPP,[23] ahora que el verdadero gas MAPP ya no está disponible.
Información adicional
- N.º ICSC: 0559
- N.º CE: 601-011-00-9
N.º de índice (clasificación y etiquetado armonizados conforme al Reglamento CLP (en:CLP_Regulation) de la UE)
Referencias
- ↑ Número CAS
- ↑ U.S. National Library of Medicine, National Center for Biotechnology Information (8 de diciembre de 2019). «Propylene compound summary» [Propileno resumen de compuesto] (en inglés). Consultado el 12 de diciembre de 2019.
- ↑ «Propylene Production from Methanol». by Intratec, ISBN 978-0-615-64811-8.
- ↑ «The reaction network in propane oxidation over phase-pure MoVTeNb M1 oxide catalysts». Journal of Catalysis 311: 369-385. 2014. doi:10.1016/j.jcat.2013.12.008. Archivado desde el original el 15 de febrero de 2016.
- ↑ Kinetic studies of propane oxidation on Mo and V based mixed oxide catalysts (en inglés). 2011.
- ↑ «Surface chemistry of phase-pure M1 MoVTeNb oxide during operation in selective oxidation of propane to acrylic acid». Journal of Catalysis 285: 48-60. 2012. doi:10.1016/j.jcat.2011.09.012. Archivado desde el original el 30 de octubre de 2016.
- ↑ «Multifunctionality of Crystalline MoV(TeNb) M1 Oxide Catalysts in Selective Oxidation of Propane and Benzyl Alcohol». ACS Catalysis 3 (6): 1103-1113. 2013. doi:10.1021/cs400010q.
- ↑ Ashford's Dictionary of Industrial Chemicals, Tercera edición, 2011, ISBN 978-0-9522674-3-0, páginas 7766-9
- ↑ «Evaluación de la seguridad del producto(PSA): Propileno». Dow Chemical Co. Archivado desde el original el 28 de agosto de 2013. Consultado el 11 de julio de 2011.
- ↑ Ghashghaee, Mohammad (2018). «Catalizadores heterogéneos para la conversión en fase gaseosa de etileno a olefinas superiores». Rev. Chem. Eng. 34 (5): 595-655. S2CID 103664623. doi:10.1515/revce-2017-0003.
- ↑ Banks, R. L.; Bailey, G. C. (1964). «Olefin Disproportionation. A New Catalytic Process». Industrial & Engineering Chemistry Product Research and Development 3 (3): 170-173.
- ↑ Lionel Delaude, Alfred F. Noels (2005). «Metátesis». Enciclopedia Kirk-Othmer de Tecnología Química (Weinheim: Wiley-VCH). ISBN 978-0471238966. doi:10.1002/0471238961.metanoel.a01.
- ↑ Schiffer, Zachary J.; Manthiram, Karthish (2017). «Electrificación y descarbonización de la industria química». Joule 1: 10-14. S2CID 117360588. hdl:1721.1/124019.
- ↑ Amghizar, Ismaël; Vandewalle, Laurien A.; Van Geem, Kevin M.; Marin, Guy B. (2017). «Nuevas tendencias en la producción de olefinas». Engineering 3 (2): 171-178.
- ↑ de Guzman, Doris (12 de octubre de 2012). «Bioenergías globales en biopropileno». Green Chemicals Blog. Archivado desde el original el 4 de noviembre de 2021. Consultado el 18 de julio de 2023.
- ↑ a b c d e f g h i j k l m n ñ o McMurry, John (2004). «Alquenos: reacciones y síntesis». Química Orgánica (sexta edición). Thompson. pp. 208-237. ISBN 970-686-354-0.
- ↑ a b McMurry, John (2004). «Éteres y epóxidos. tioles y sulfuros». Química Orgánica (sexta edición). Thompson. pp. 648-649. ISBN 970-686-354-0.
- ↑ Beyer, Walter (1987). «Compuestos alinfáticos». Manual de química orgánica (19º edición). Reverté. p. 79. ISBN 84-291-7066-9.
- ↑ Yúfera, Eduardo Primo (1996). «Hidrocarburos III. Alquenos». Química orgánica básica y aplicada:de la molécula a la industria (Volumen 1). Reveté. pp. 158-159. ISBN 84-291-7953-4.
- ↑ a b «Estudio de mercado: Propileno (2ª edición), Ceresana, diciembre de 2014». ceresana.com. Consultado el 3 de febrero de 2015.
- ↑ Merck & Co., ed. (1996). «8034. Propileno». El Índice Merck, duodécima edición. Nueva Jersey. pp. 1348-1349.
- ↑ J.G.L., Fierro (Ed.) (2006). Óxidos metálicos, química y aplicaciones. CRC Press. pp. 414-455.
- ↑ Por ejemplo, "MAPP-Pro"
Enlaces externos
- https://www.ilo.org/dyn/icsc/showcard.display?p_lang=es&p_card_id=0559 Ficha ICSC del propileno en el sitio web de la Organización Internacional del Trabajo










![{\displaystyle {\ce {CH2=CH2{}+CH3CH=CHCH3->[][{\text{Re, Mo}} \atop {\text{catalyst}}]2CH2=CHCH3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/acdd4b00da58144bb78872e0663521fe689b07b1)